Kimyasal Bağlar
Kimyasal bağlar, atomların bir arada durmasını sağlayan ve maddenin temel özelliklerini belirleyen etkileşimlerdir. Başlıca iyonik, kovalent ve metalik bağlar olmak üzere üç ana türü vardır.
İyonik Bağ
Örnek: NaCl (Sodyum Klorür)
- Metal (Na) ile ametal (Cl) arasında oluşur
- Elektron transferi ile gerçekleşir
- Na → Na⁺ + e⁻ (katyon)
- Cl + e⁻ → Cl⁻ (anyon)
- Zıt yüklü iyonların elektrostatik çekimi
- Bağ enerjisi: 787 kJ/mol (yüksek)
- Özellikler: Sert, kırılgan, yüksek erime noktası, suda çözünür
Kovalent Bağ
Elektronların ortaklaşa kullanımı ile oluşur. İki ana türü vardır:
Polar Kovalent Bağ
Örnek: H₂O (Su)
- Farklı elektronegatiflikte atomlar arasında
- Elektronlar eşit paylaşılmaz
- Kısmi pozitif (δ+) ve negatif (δ-) yükler oluşur
- Bağ enerjisi: 464 kJ/mol (O-H bağı)
Apolar Kovalent Bağ
Örnek: CH₄ (Metan)
- Aynı veya benzer elektronegatiflikte atomlar arasında
- Elektronlar eşit paylaşılır
- Yük dağılımı simetriktir
- Bağ enerjisi: 413 kJ/mol (C-H bağı)
Metalik Bağ
Örnek: Cu (Bakır)
- Metal atomları arasında
- "Denizde elektron bulutu" modeli
- Değerlik elektronları serbestçe hareket eder
- Bağ enerjisi: Değişken (metale göre)
- Özellikler: Elektrik iletkenliği, süneklik, parlaklık
Moleküller Arası Etkileşimler (Zayıf Bağlar)
| Etkileşim Türü | Enerji (kJ/mol) | Örnek | Açıklama |
|---|---|---|---|
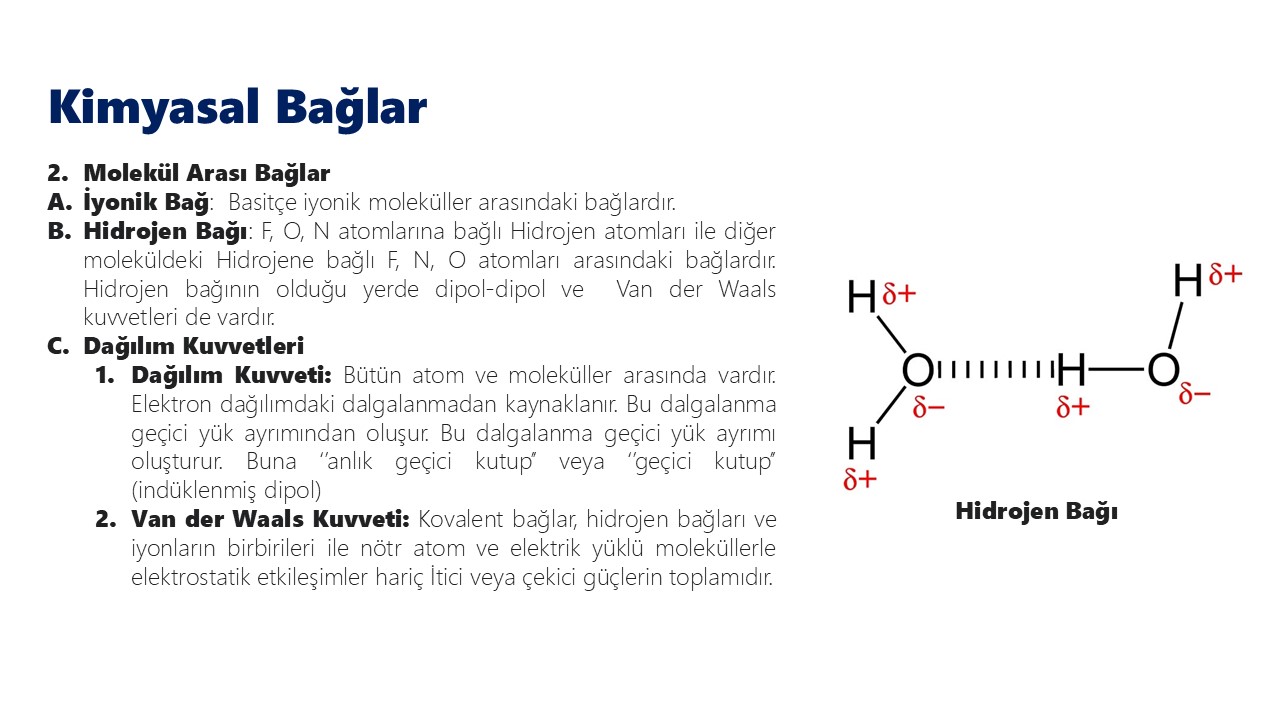
| Hidrojen Bağı | 10-40 | H₂O, NH₃, HF | H ile N,O,F arasında, en güçlü zayıf bağ |
| Dipol-Dipol | 5-20 | HCl, CO | Polar moleküller arası çekim |
| London Kuvvetleri | 1-10 | CH₄, Ar | Geçici dipoller arası, tüm maddelerde var |
Hidrojen Bağı Özel Durumu
Hidrojen bağı, suyun olağanüstü özelliklerinden sorumludur:
- Erime/Donma noktası: 0°C (beklenenden yüksek)
- Kaynama noktası: 100°C (beklenenden yüksek)
- Özgül ısı kapasitesi: 4.18 J/g°C (çok yüksek)
- Buzun yoğunluğu: Sıvı sudan az (eşsiz özellik)
Bağ Kuvvetleri Karşılaştırması
- İyonik/Kovalent Bağlar: 150-1100 kJ/mol (en güçlü)
- Metalik Bağlar: 75-400 kJ/mol
- Hidrojen Bağları: 10-40 kJ/mol
- Dipol-Dipol: 5-20 kJ/mol
- London Kuvvetleri: 1-10 kJ/mol (en zayıf)
Uygulama Alanı
Soru 1: Aşağıdaki moleküllerden hangisinde hidrojen bağı oluşabilir? a) CH₄ b) NH₃ c) HCl d) H₂S
Soru 2: CO₂ molekülünde hangi tür bağlar bulunur? Moleküller arası etkileşimi nedir?
Soru 3: Aşağıdaki maddeleri kaynama noktalarına göre artan sırada düzenleyiniz: CH₄, H₂O, NaCl, Ar
Soru 4: Metallerin elektriği iletmesinin nedeni nedir?
Soru 5: HF'nin kaynama noktası (19.5°C), HCl'ninkinden (-85°C) çok daha yüksektir. Neden?
Önemli Uyarılar
- Hidrojen bağı sadece H-N, H-O veya H-F bağları içeren moleküllerde oluşur
- London kuvvetleri molekül büyüdükçe artar (C₅H₁₂ > CH₄)
- İyonik bileşikler katı halde elektriği iletmez, sadece sıvı halde veya çözeltide iletir
- Kovalent ağ yapılı maddeler (elmas, SiO₂) çok yüksek erime noktasına sahiptir